L’imagerie joue un rôle majeur dans l’évaluation objective de la réponse tumorale aux traitements anticancéreux. En routine clinique, le clinicien base sa décision de poursuivre ou d’arrêter son traitement essentiellement sur l’évolution des tumeurs en imagerie. Dans les essais cliniques, c’est en partie à partir de l’évaluation en imagerie qu’est déterminée l’efficacité des traitements qui sont ensuite approuvés pour une mise sur le marché par les autorités réglementaires. C’est dans ce contexte que la communauté nationale a mis au point des critères standardisés en imagerie d’évaluation des traitements en oncologie. Il est de notre responsabilité en tant que communauté – envers les patients atteints de cancer et nos collègues cliniciens les prenant en charge – de nous assurer que nos techniques d’imagerie soient fiables et robustes, et que les radiologues soient formés pour les interpréter, car beaucoup de décisions thérapeutiques dépendront de nos évaluations.
Des critères internationaux standardisés
La plupart des méthodes d’évaluation des traitements sont basées sur la mesure de la taille des lésions. Les critères RECIST [1] (Response Evaluation Criteria in Solid Tumors), développés en 2000 et révisés en 2009, sont devenus les critères les plus largement utilisés pour l’évaluation de la réponse dans les essais cliniques dans les tumeurs solides.
Pour les lymphomes, ce sont les critères de l’IWG [2] (International Working Group), dits critères de Cheson, qui sont utilisés pour évaluer l’efficacité thérapeutique. Ils sont basés sur la mesure bi-dimensionnelle (le plus grand axe et sa plus grande perpendiculaire) des lésions, et prennent en compte le métabolime tumoral en intégrant la tomographie par émission de positons (TEP).
D’autres critères ont été développés en fonction des besoins, mais sont moins systématiquement utilisés. Les critères de Choi [3] dans les tumeurs stromales gastro-intestinales (GIST) sous imatinib prennent en compte à la fois les changements de taille et la nécrose mesurée par la densité en scanner. Les critères mRECIST [4] sont utilisés dans les carcinomes hépatocellulaires traités par chimio-embolisation, et ne mesurent que la portion viable hypervasculaire des lésions.
Enfin, derniers arrivés, les critères iRECIST [5] pour évaluer les immunothérapies ont été développés par le groupe RECIST et publiés en mars 2017. Cette nouvelle classe thérapeutique a démontré leur efficacité dans les mélanomes et les cancers du poumon. De nombreux essais cliniques sont en cours dans d’autres cancers. Cependant, ces traitements posent de nouveaux problèmes d’évaluation de la réponse au traitement car 10% environ des patients ont une réaction initiale immunitaire majeure, entraînant une augmentation massive de la taille des lésions, pouvant être prise à tort pour une progression, alors que ces patients répondront ensuite au traitement.
Comment former les radiologues ?
La communauté radiologique est très active pour former les radiologues à ces critères, afin d’harmoniser la prise en charge sur le territoire national. Il est indispensable pour l’ensemble des radiologues de maîtriser ces outils, car les patients oncologiques représentent un grand nombre de nos patients, que ce soit en activité libérale ou hospitalière.
Une formation de DPC (Développement Professionnel Continu) a été mise ne place par l’ODPCRIM dès 2013 afin de former les radiologues à l’utilisation de ces critères d’évaluation de la réponse tumorale. Dans le cadre de l’initiative de FORCE imaging, qui vise à structurer l’imagerie dans la recherche clinique, un atelier « Hands on » va être organisé au premier trimestre 2018 afin de proposer une formation pratique centrée sur des cas cliniques. Des initiatives similaires sont en cours au niveau européen, en lien avec l’ESOI (European Society of Oncologic Imaging) et l’EORTC (European Organisation for Research and Treatment of Cancer).
Conclusion
Ces critères ont été développés pour les protocoles d’essais thérapeutiques, pour pouvoir comparer l’efficacité de différentes drogues entre elles. Cependant, ils peuvent être utiles pour le praticien au quotidien, car ils fournissent une trame de lecture des examens et de rédaction de comptes-rendus, impliquant la mesure des mêmes lésions sur les examens successifs, et une conclusion globale, afin d’améliorer la lisibilité pour les cliniciens. Des critères reproductibles, objectifs et quantitatifs sont nécessaires pour définir un langage commun entre les radiologues et les cliniciens, afin que ces derniers puissent prendre une décision thérapeutique éclairée.
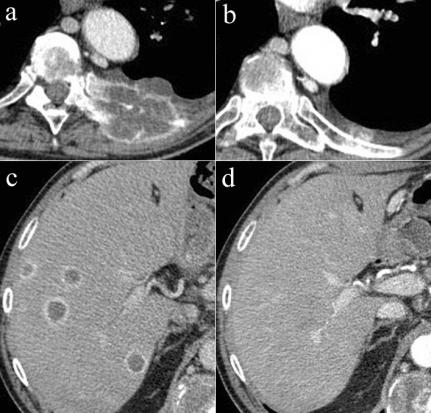
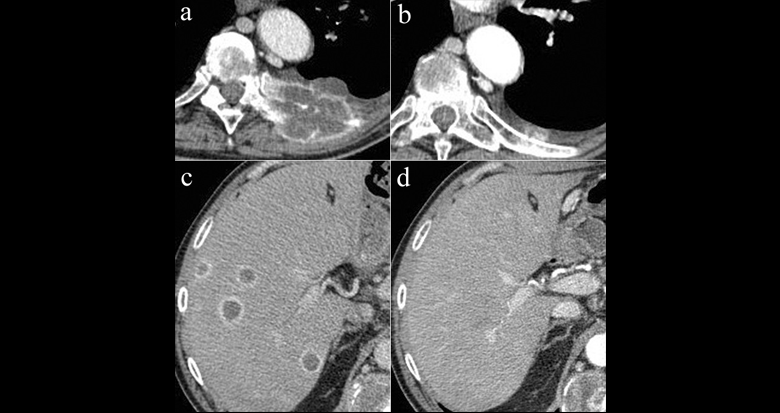
Figure 1. Patient porteur d’un cancer du rein métastatique sous traitement évalué selon les critères internationaux, montrant une très bonne réponse au traitement. Coupes axiales de scanner d’une métastase envahissant l’arc postérieur de la 9ème côte gauche et de multiples métastases hépatiques respectivement avant traitement (a, b) puis après traitement (c, d) avec diminution importante de taille de la lésion costale et disparition complète des lésions hépatiques.
- Eisenhauer EA, Therasse P, Bogaerts J, Schwartz LH, Sargent D, Ford R, Dancey J, Arbuck S, Gwyther S, Mooney M, Rubinstein L, Shankar L, Dodd L, Kaplan R, Lacombe D, Verweij J. New response evaluation criteria in solid tumours: revised RECIST guideline (version 1.1). Eur J Cancer. 2009 Jan;45(2):228-47.
- Cheson BD. Staging and response assessment in lymphomas: the new Lugano classification. Chin Clin Oncol. 2015 Mar;4(1):5.
- Choi H, Charnsangavej C, Faria SC, Macapinlac HA, Burgess MA, Patel SR, Chen LL, Podoloff DA, Benjamin RS. Correlation of computed tomography and positron emission tomography in patients with metastatic gastrointestinal stromal tumor treated at a single institution with imatinib mesylate: proposal of new computed tomography response criteria. J Clin Oncol. 2007 May 1;25(13):1753-9.
- Lencioni R, Llovet JM. Modified RECIST (mRECIST) assessment for hepatocellular carcinoma. Semin Liver Dis. 2010 Feb;30(1):52-60.
- Seymour L, Bogaerts J, Perrone A, Ford R, Schwartz LH, Mandrekar S, Lin NU, Litière S, Dancey J, Chen A, Hodi FS, Therasse P, Hoekstra OS, Shankar LK, Wolchok JD, Ballinger M, Caramella C, de Vries EG; RECIST working group. IRECIST: guidelines for response criteria for use in trials testing
- immunotherapeutics. Lancet Oncol. 2017 Mar;18(3):e143-e152.
Laure FOURNIER 1,2
1. Assistance Publique-Hôpitaux de Paris, HEGP, Service de Radiologie. 2 Université Paris Descartes Sorbonne Paris Cité, INSERM UMR-S970
En savoir +
Séance pédagogique
Bilan de la carcinose péritonéale: une histoire de couple radiologue-chirurgien