Même si la localisation sous-cutanée des testicules facilite l’examen clinique, ce dernier peut être pris en défaut : par exemple certaines tumeurs ne sont pas palpables. Les tumeurs germinales (95 % des tumeurs testiculaires) peuvent être de nature séminomateuses (TGS) ou non-séminomateuses (TGNS). Les marqueurs tumoraux (HcG, AFP, LDH), quand ils sont positifs (ce qui oriente vers le diagnostic de TGNS), aident au diagnostic. Les biopsies percutanées ne sont pas recommandées par les sociétés savantes (par peur d’essaimage), et l’orchidectomie totale est le traitement préconisé en cas de suspicion de tumeur. Cette attitude quelque peu dogmatique est de plus en plus remise en question, car des orchidectomies totales sont effectuées par excès, révélant des tumeurs bénignes comme des tumeurs stromales à cellules de Leydig, diagnostic différentiel principal devant une lésion nodulaire vascularisée, ou encore des lésions non tumorales. La caractérisation par l’imagerie a donc un rôle crucial.
Les Ultrasons
Le mode B
L’examen permet de mesurer le volume de chaque testicule, d’analyser son échostructure. Le testicule normal est homogène, en dehors du hile hyperéchogène. La pathologie tumorale germinale ou stromale se présente sous la forme de nodule, de masse, possiblement lobulée, hypoéchogène dans la grande majorité des cas. Cette hypoéchogénicité n’est pas spécifique et ne permet pas la caractérisation. La présence de microlithes groupés/ microlithiase/macrocalcification en association à des nodules oriente plutôt vers une tumeur germinale. Le caractère mal défini, très hypoéchogène, la multiplicité, la grande taille (> 1 cm) sont des éléments également péjoratifs. Les très petits testicules symétriques (2 ml) avec micronodules sont évocateurs de syndrome de Klinefleter et ne sont pas chirurgicaux.
Le Doppler Couleur et le Doppler ultrasensible
Le Doppler couleur doit être optimisé pour la détection des flux lents, ce qui permet d’apprécier la vascularisation du nodule. Cette visualisation dépend bien sûr de sa sensibilité. Le Doppler ultrasensible permet une meilleure résolution spatiale des petits vaisseaux : l’architecture vasculaire est à dominante transnodulaire dans les tumeurs germinales, et circonférentielle dans les tumeurs à cellule de Leydig. La diminution de la vascularisation est en faveur d’une involution fibreuse (« burned out tumors »).
L’élastographie ultrasonore
Cette évaluation de la dureté des tissus peut s’effectuer par compressions itératives manuelles (Strain Elastography, SE), ou par ondes de cisaillement (Shear Wave Elastography), L’échelle et les ratios par rapport au parenchyme sain doivent toujours être mentionnés. Les tumeurs malignes sont plus dures que les lésions bénignes mais il y a des chevauchements de valeurs entre les lésions bénignes et malignes. Par exemple le kyste dermoïde, lésion bénigne, fait partie des lésions les plus dures. Dans les testicules avec des plages mal définies, une augmentation focale de la dureté doit faire suspecter une « burned out tumor » et réaliser une IRM.
L’échographie de contraste
L’injection intraveineuse de microbulles permet de sensibiliser la détection de vascularisation avec plus de sensibilité par rapport à l’écho-Doppler. L’absence de rehaussement des kystes dermoïdes, et la nette diminution de vascularisation des « burned-out tumors » seront plus évidentes, surtout si on ne dispose pas d’un Doppler très sensible. Concernant la quantification du rehaussement des lésions vascularisées, il n’y a que peu d’études, et leurs résultats sont contradictoires.
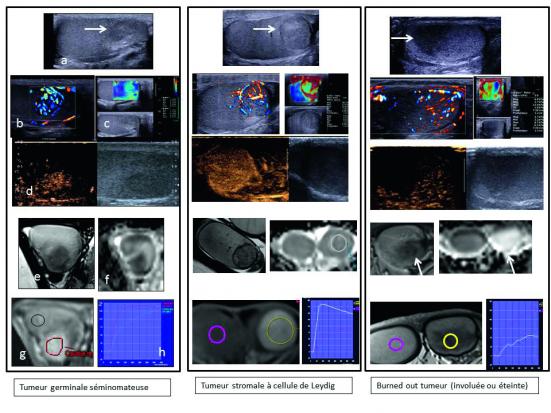
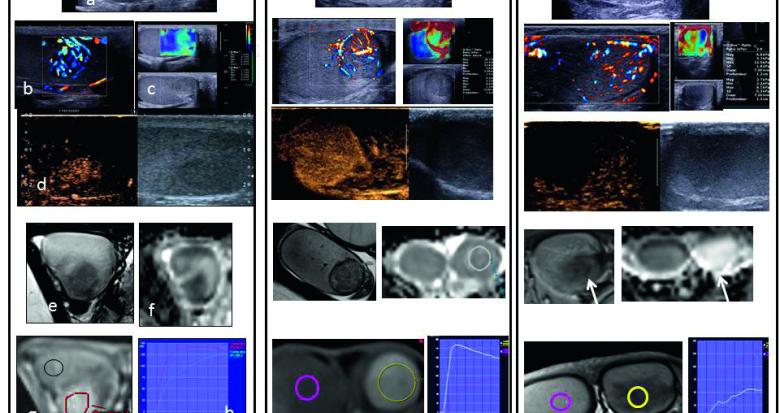
Fig. 1. Exemples de l’imagerie multiparamétrique de trois lésions : une tumeur germinale séminomateuse, une tumeur stromale à cellule de Leydig, et une « burned-out tumor », découvertes sur des bilans d’infertilité, dont la prise en charge diffère : les tumeurs germinales et les « burned-out tumor » doivent faire l’objet d’une orchidectomie. Les tumeurs à cellule de Leydig peuvent faire l’objet soit d’une surveillance en cas de petite taille (< 5 mm), soit d’une chirurgie de préférence partielle. a : mode B, b : Doppler couleur (ultrasensible pour les deux dernières lésions), c : élastographie par onde de cisaillement , d : échographie de contraste, e : IRM pondérée en T2, f : cartographie ADC, g : T1 par injection de Gadolinium avec courbes de rehaussement.
L’IRM
L’IRM est indiquée dans la caractérisation des lésions incertaines : lésions non palpables à marqueurs normaux, doute sur le caractère extra ou intra-testiculaire d’une masse, suspicion de « burned-out tumor » devant une plage d’allure tumorale, hypo ou avasculaire en Doppler couleur. Elle doit comprendre des séquences T1, T2, en diffusion, et des séquences dynamiques après injection de produit de contraste.
Les testicules sont en hypersignal homogène en T2. Le caractère nodulaire, en hyposignal T2 et un rehaussement évoque un processus tumoral. Les tumeurs germinales comme les tumeurs à cellules de Leydig présentent une restriction en diffusion, mais les tumeurs bénignes à cellules de Leydig ont en moyenne une restriction moins importante.
L’IRM dynamique avec courbes de rehaussement montre que les tumeurs à cellules de Leydig présentent un rehaussement plus précoce et intense que les tumeurs séminomateuses. Pour les « burned-out tumors », une lésion nodulaire nette est identifiée en T2, très faiblement vascularisée, avec une restriction plus faible que le parenchyme sain (ADC élevé).
Laurence Rocher
APHP, Hôpitaux Paris Sud, site Bicêtre, Service de Radiologie diagnostique et interventionnelle du Pr MF Bellin
IR4M Imagerie par Résonance Magnétique Médicale et Multi-Modalités, BIOMAPS, SHFJ, Orsay
Faculté de Médecine Paris Sud, Le Kremlin-Bicêtre
Bertrand Bresson
APHP, Hôpitaux Paris Sud, site Bicêtre, Service de Radiologie diagnostique et interventionnelle du Pr MF Bellin
IR4M Imagerie par Résonance Magnétique Médicale et Multi-Modalités, BIOMAPS, SHFJ, Orsay
Faculté de Médecine Paris Sud, Le Kremlin-Bicêtre
Florian Maxwell
APHP, Hôpitaux Paris Sud, site Bicêtre, Service de Radiologie diagnostique et interventionnelle du Pr MF Bellin
Faculté de Médecine Paris Sud, Le Kremlin-Bicêtre
Ghina Hindawi
APHP, Hôpitaux Paris Sud, site Bicêtre, Service de Radiologie diagnostique et interventionnelle du Pr MF Bellin
Cristina Balasa
APHP, Hôpitaux Paris Sud, site Bicêtre, Service de Radiologie diagnostique et interventionnelle du Pr MF Bellin
En savoir +
Séance pédagogique
Pourquoi utiliser l’échographie multiparamétrique en oncologie ?